Two redundant transcription factor binding sites in a single enhancer are essential for mammalian sex determination
Meshi Ridnik , Elisheva Abberbock, Veronica Alipov, Shelly Ziv Lhermann, Shoham Kaufman, Maor Lubman, Francis Poulat, Nitzan Gonen
Génétique, biologie cellulaire et développement
Le développement de l’appareil reproducteur nécessite une détermination/différenciation des gonades embryonnaires et une maturation des organes reproducteurs, hautement coordonnées et régulées. Les anomalies de ces processus pendant le développement embryonnaire précoce, en raison de facteurs génétiques ou environnementaux, induiront un large éventail de syndromes appelés «troubles du développement sexuel» (TDS), allant de la dysgénésie gonadique complète (inversion sexuelle), du gonadoblastome au phénotype moins sévère de la cryptorchidie (testicule non descendu).
Les gonades embryonnaires proviennent d'un primordium bipotentiel (la crête génitale) qui peut se différencier en un testicule ou un ovaire via l'action de différents facteurs de transcription. Dans l'embryon de souris, la détermination du sexe se produit entre le jour embryonnaire (E)10.5 et E12.5 dans la crête génitale par la différenciation des progéniteurs en une population cellulaire spécifique, les cellules de soutien. Ces cellules vont ensuite organiser morphologiquement les gonades embryonnaires et induire la détermination du sexe de la lignée germinale.
Chez les mâles, la différenciation des cellules de soutien, appelées cellules de Sertoli, est initiée par l'expression du gène Sry présent sur le chromosome Y, qui active l’expression du gène autosomique Sox9, un membre de la famille du groupe SOX E. En l'absence de Sry chez les femelles, les progéniteurs se différencient en cellules de granulosa, la lignée cellulaire de soutien femelle. Alors que Sry est l’inducteur de la cascade mâle, Sox9 est considéré comme le principal effecteur en aval de Sry dans le processus de différenciation cellulaire de la cellule de Sertoli. Après son activation par Sry, le maintien de l'expression du gène Sox9 est un événement clé dans le programme de différenciation sexuelle chez les mammifères. Dans la gonade XY de souris, Sox9 active l’expression de Fgf9, induisant une boucle de régulation Sox9/Fgf9 (pour revue (1)).
Notre équipe a identifié la prostaglandine D2 (PGD2) (Figure 1) qui est produite par les prostaglandine D- et H- synthases (Ptgds1 et 2 respectivement) et qui active la translocation nucléaire SOX9 (2) et l'expression de la transcription du gène Sox9, agissant comme une deuxième boucle d’amplification et de maintien de la voie mâle (3,4). La voie de signalisation PGD2 contribue également à la différenciation des cellules germinales embryonnaires mâles (5), puis à la régulation du pool de cellules souches spermatogoniales dans le testicule postnatal.
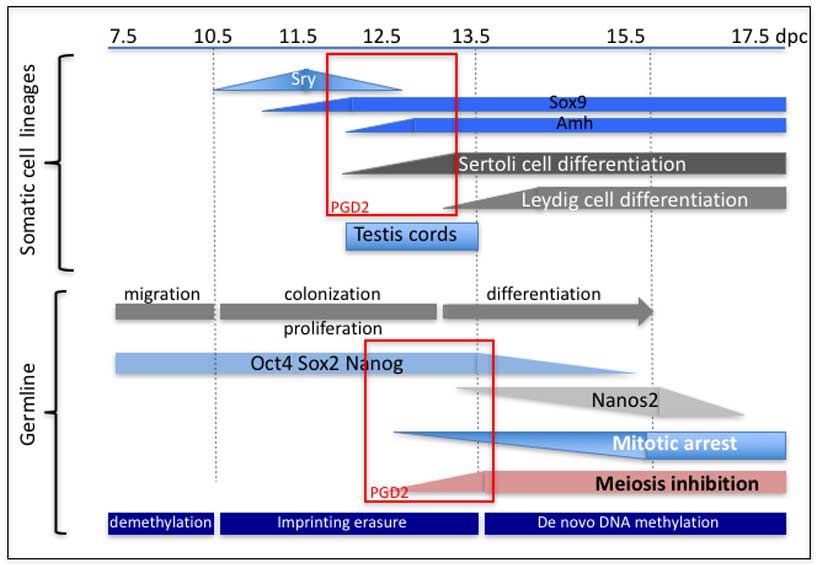
Figure 1 : la signalisation PGD2 est impliquée dans la différenciation somatique et des cellules germinales du testicule embryonnaire
La synthèse des prostaglandines est inhibée par les anti-inflammatoires non stéroïdiens (AINS) et les médicaments analgésiques, tels que le paracétamol (acétaminophène: ACE), largement utilisés par les femmes enceintes. Sur la base des résultats d’études épidémiologiques, un lien potentiel entre TDS et exposition à de telles molécules au cours des premier et deuxième trimestres de gestation a été suggéré. Nous avons démontré que les gonades embryonnaires sont affectées après leur exposition in utero à l'ACE, l'aspirine et/ou l'ibuprofène à des doses thérapeutiques, similaires à celles administrées à l’homme. La différenciation anticipée de la lignée germinale embryonnaire mâle est induite, affectant le pool de cellules souches spermatogoniales dans le testicule postnatal et le nombre de spermatozoïdes des testicules adultes des générations F1 et F2, suggérant un impact transgénérationnel de ces drogues.
Sox9 étant le principal gène déterminant le sexe chez les mammifères et dans l'objectif d'identifier les réseaux génétiques directement régulés par Sox9, nous avons combiné l'analyse des régions de chromatine liées à Sox9 dans les testicules foetaux murins et bovins avec le séquençage d'ARN de testicules de souris invalidés pour Sox9. Nous avons montré que Sox9 contrôle un programme génétique conservé qui implique la plupart des gènes de la détermination du sexe. Dans les testicules fœtaux, Sox9 module à la fois la transcription et directement ou indirectement l'épissage différentiel spécifique du sexe de ses gènes cibles en se liant à des régions génomiques via des motifs séquentiels conservés chez les mammifères et que nous appelons 'Sertoli Cell Signature' (SCS). La SCS se caractérise par une organisation précise des motifs de fixation des facteurs de reprogrammation des cellules Sertoli Sox9, Gata4 et Dmrt1. À partir de l'hypothèse selon laquelle les facteurs nucléaires qui se lient aux régions génomiques avec SCS pourraient fonctionnellement interagir avec SOX9, nous avons identifié Trim28 (Figure 2), un nouveau partenaire Sox9 dans les testicules fœtaux (6).
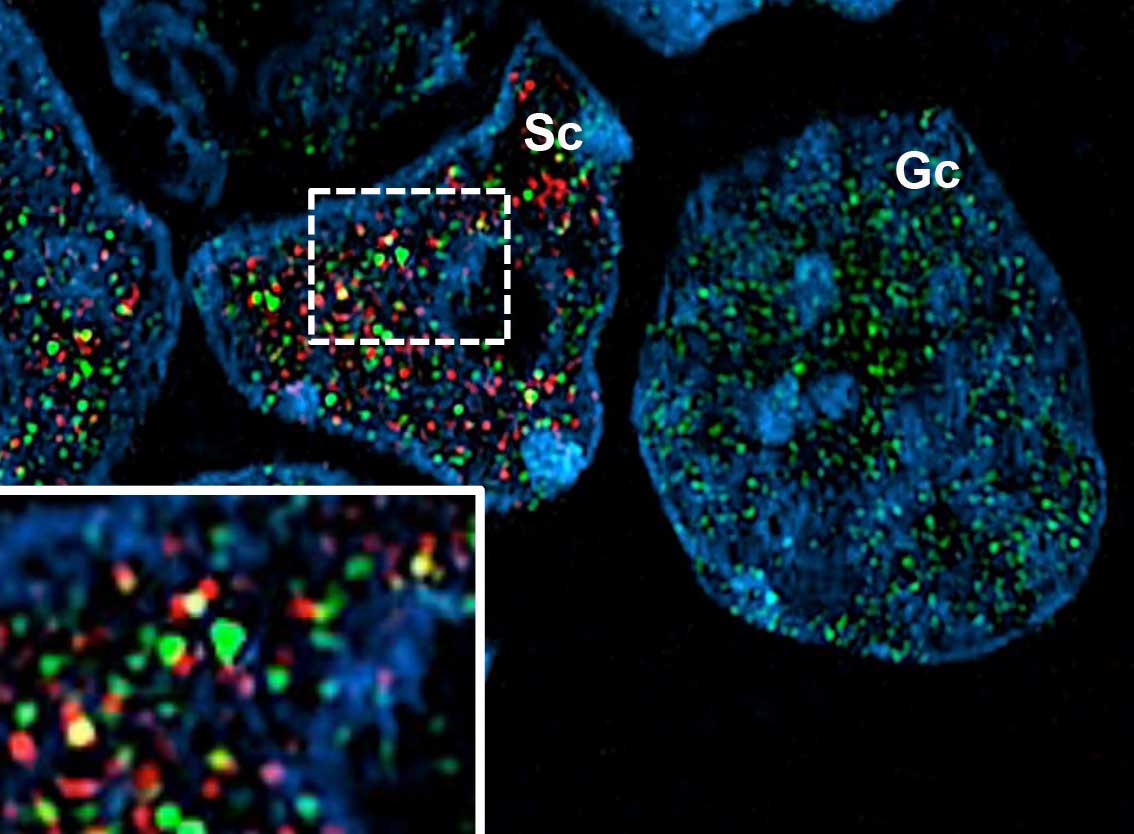
Figure 2 : microscopie à fluorescence OMX de super résolution (sections Z de 0,12 μm) montrant la co-localisation de Sox9 (rouge) et Trim28 (vert) dans le noyau de cellules E13.5 Sertoli (points orange / jaune indiqués par des flèches blanches dans l’insert). ADN (bleu). Sc: cellules de Sertoli; Gc: cellules germinales. Barre: 2μm.
Meshi Ridnik , Elisheva Abberbock, Veronica Alipov, Shelly Ziv Lhermann, Shoham Kaufman, Maor Lubman, Francis Poulat, Nitzan Gonen
Isabelle Stevant Nitzan Gonen Francis Poulat
Pascal Philibert, Stéphanie Déjardin, Mélissa Girard, Quentin Durix, Anne-Alicia Gonzalez, Xavier Mialhe, Mathieu Tardat, Francis Poulat, Brigitte Boizet-Bonhoure
Moïra Rossitto , Stephanie Déjardin , Chris M Rands , Stephanie Le Gras , Roberta Migale , Mahmoud-Reza Rafiee , Yasmine Neirijnck , Alain Pruvost , Anvi Laetitia Nguyen , Guillaume Bossis , Florence Cammas , Lionel Le Gallic , Dagmar Wilhelm , Robin Lovell-Badge , Brigitte Boizet-Bonhoure , Serge Nef , Francis Poulat
B. Boizet-Bonhoure, S. Dejardin, M. Rossitto, F. Poulat and P. Philibert
Rossitto M, Ollivier M, Déjardin S, Pruvost A, Brun C, Marchive C, Nguyen AL, Ghettas A, Keime C, de Massy B, Poulat F, Philibert P, Boizet-Bonhoure B
Weger BD, Gobet C, Yeung J, Martin E, Jimenez S, Betrisey B, Foata F, Berger B, Balvay A, Foussier A, Charpagne A, Boizet-Bonhoure B, Chou CJ, Naef F, Gachon F
van Dijk J, Bompard G, Cau J, Kunishima S, Rabeharivelo G, Mateos-Langerak J, Cazevieille C, Cavelier P, Boizet-Bonhoure B, Delsert C, Morin N
Rossitto M, Marchive C, Pruvost A, Sellem E, Ghettas A, Badiou S, Sutra T, Poulat F, Philibert P, Boizet-Bonhoure B

Gonen N, Futtner CR, Wood S, Garcia-Moreno SA, Salamone IM, Samson SC, Sekido R, Poulat F, Maatouk DM, Lovell-Badge R
Penrad-Mobayed M, Perrin C, L'Hôte D, Contremoulins V, Lepesant JA, Boizet-Bonhoure B, Poulat F, Baudin X, Veitia RA
Rahmoun M, Lavery R, Laurent-Chaballier S, Bellora N, Philip GK, Rossitto M, Symon A, Pailhoux E, Cammas F, Chung J, Bagheri-Fam S, Murphy M, Bardwell V, Zarkower D, Boizet-Bonhoure B, Clair P, Harley VR, Poulat F.
Boizet-Bonhoure, B.
Rossitto M, Philibert P, Poulat F, Boizet-Bonhoure B.
Rossitto M, Ujjan S, Poulat F, Boizet-Bonhoure B
Trimarco A, Forese MG, Alfieri V, Lucente A, Brambilla P, Dina G, Pieragostino D, Sacchetta P, Urade Y, Boizet-Bonhoure B, Boneschi FM, Quattrini A, Taveggia C.
Rahmoun M, Perez J, Saunders PA, Boizet-Bonhoure B, Wilhelm D, Poulat F, Veyrunes F.
Moniot B, Ujjan S, Champagne J, Hirai H, Aritake K, Nagata K, Dubois E, Nidelet S, Nakamura M, Urade Y, Poulat F, Boizet-Bonhoure B
Philibert P, Boizet-Bonhoure B, Bashamboo A, Paris F, Aritake K, Urade Y, Leger J, Sultan C, Poulat F.
Lichten, M., de Massy, B.
Moniot B, Farhat A, Aritake K, Declosmenil F, Nef S, Eguchi N, Urade Y, Poulat F, Boizet-Bonhoure B.
Sim H, Argentaro A, Czech DP, Bagheri-Fam S, Sinclair AH, Koopman P, Boizet-Bonhoure B, Poulat F, Harley VR
Dumond, H., Al-Asaad, I., Chesnel, A., Chardard, D., Boizet-Bonhoure, B., Flament, S., Kuntz, S.
Farhat A, Philibert P, Sultan C, Poulat F, Boizet-Bonhoure B.
Abdel-Samad R, Zalzali H, Rammah C, Giraud J, Naudin C, Dupasquier S, Poulat F, Boizet-Bonhoure B, Lumbroso S, Mouzat K, Bonnans C, Pignodel C, Raynaud P, Fort P, Quittau-Prévostel C, Blache P
Lakhdar R, Denden S, Knani J, Leban N, Daimi H, Hassine M, Lefranc G, Ben Chibani J, Haj Khelil A.
+
IMGT® - le système d'information international en ImMunoGénéTique
Malki S, Boizet-Bonhoure B, Poulat F
Kalfa N, Méduri G, Philibert P, Patte C, Boizet-Bonhoure B, Thibaut E, Pienkowski C, Jaubert F, Misrahi M, Sultan C.
Malki S, Boizet-Bonhoure B, Poulat F
Kalfa, N., Veitia, RA., Benayoun, BA., Boizet-Bonhoure, B., Sultan, C.
Kalfa, N., Philibert, P., Sultan, C
Kalfa, N., Philibert, P., Sultan, C.
Moniot, B., Declosmenil, F, Barrionuevo, F., Scherer, G., Aritake, K., Malki, S., Marzi, M., Cohen-Solal, A., Georg, I., Klattig, J., Englert, C., Kim, Y., Capel, B., Eguchi, N., Urade, Y., Boizet-Bonhoure, B., Poulat, F.
Kalfa N, Philibert P, Patte C, Thibaud E, Pienkowski C, Ecochard A, Boizet-Bonhoure B, Fellous M, Sultan C.
Moniot, B., Boizet-Bonhoure, B., Poulat, F.
Malki, S., Declosmenil, F., Farhat, A., Moniot, B., Poulat, F., Boizet-Bonhoure, B.
Kalfa, N., M. Fellous, B. Boizet-Bonhoure, C. Patte, P. Duvillard, C. Pienkowski, F. Jaubert, A. Ecochard and C. Sultan.
El Jamil, A., Kanhoush, R., Magre, S., Boizet-Bonhoure, B., Penrad-Mobayed, M.
Manuylov, NL., Fujiwara, Y., Adameyko, II., Poulat, F., Tevosian, SG.
Malki, S., Bibeau, F., Notarnicola, C., Roques, S., Berta, P., Poulat, F., Boizet-Bonhoure, B.
Galmiche, L., Sarnacki, S., Verkarre, V., Boizet, B. Duvillie, B., Fabre, M., Jaubert, F
Köhler, B., Delezoide, AL., Boizet-Bonhoure, B., McPhaul, MJ., Sultan, C., Lumbroso, S
Kim, Y., Kobayashi, A., Sekido, R., DiNapoli, L., Brennan, J., Chaboissier, M.C., Poulat, F., Behringer, R.R., Lovell-Badge, R. and Capel, B.
Notarnicola C, Malki S, Berta P, Poulat F, Boizet-Bonhoure B.
Notarnicola C, Malki S, Berta P, Poulat F, Boizet-Bonhoure B.
Malki, S., Berta, P., Poulat, F., Boizet-Bonhoure, B.
Malki, S., Nef, S., Notarnicola, C., Thevenet, L., Gasca, S., Méjean, C., Berta, P., Poulat, F., Boizet-Bonhoure, B.
Nef, S., Schaad, O., Stallings, N.R., Cederroth, C.R., Pitetti, J.L., Schaer, G., Malki, S., Dubois-Dauphin, M., Boizet-Bonhoure, B., Descombes, P., Parker, K.L. and Vassalli, J.D.
Thevenet, L., Albrecht, K.H., Malki, S., Berta, P., Boizet-Bonhoure, B. and Poulat, F.
Thevenet, L., Mejean, C., Moniot, B., Bonneaud, N., Galeotti, N., Aldrian-Herrada, G., Poulat, F., Berta, P., Benkirane, M., Boizet-Bonhoure, B.
Moniot, B., Biau, S., Faure, S., Nielsen, C.M., Berta, P., Roberts, D.J. and de Santa Barbara, P.
Zhou, R., Bonneaud, N., Yuan, C., de Santa Barbara, P., Boizet, B., Schomber, T., Scherer, G., Roeder, G., Poulat, F., Berta, P.
Hardelin, J.P., Julliard, A.K., Moniot, B., Soussi-Yanicostas, N., Verney, C., Schwanzel, M., Ayer-Le-Lièvre, C. and Petit, C.
Soutenue par Moïra Rossitto le 09-12-2016
